از چاپ رگهای خونی تا ساخت اندام روی تراشه
علی خادمحسینی یکی از نامدارترین دانشمندان ایرانی فعال در این حوزه علمی است که هافینگتونپست او را رهبر جهانی در حوزه زیستمواد و مهندسی بافت معرفی کرده است. خادمحسینی استاد دانشگاه هاروارد و بخش مشترک علوموفناوری دانشگاه هاروارد و MIT و همچنین مدیر مرکز نوآوری مواد زیستی در بیمارستان بیرگام و زنان (Brigham and Women’s Hospital) است، مرکزی که در آنجا پروژههای بزرگی را با حضور بیش از ۹۰ محقق هدایت میکند. او پژوهشگر مهندسی مواد زیستی، طب احیاشونده، بافت یا اندام روی تراشه و بسیاری از دیگر پروژههای مرتبط با پزشکی و مهندسی بافت و عضو رسمی موسسه مهندسی زیستی و پزشکی آمریکا، انجمن سلطنتی شیمی بریتانیا و انجمن علوم پیشرفته آمریکاست. ساخت رگهای خونی با استفاده از چاپگرهای سهبعدی در سال ۱۳۹۳/۲۰۱۴ یکی از بزرگترین موفقیتهای این دانشمند ایرانی ساکن آمریکاست که در گفتوگو با «دانشمند» جزئیاتی را درباره این پروژه و دیگر کارهای در دست اجرایش ارائه کرده است.
میتوانید درباره پژوهشهای جدیدتان در زمینه مهندسی نسوج، مثلا نحوه چاپ سهبعدی عروق خونی یا ساخت مدل اندام روی تراشه توضیح دهید؟
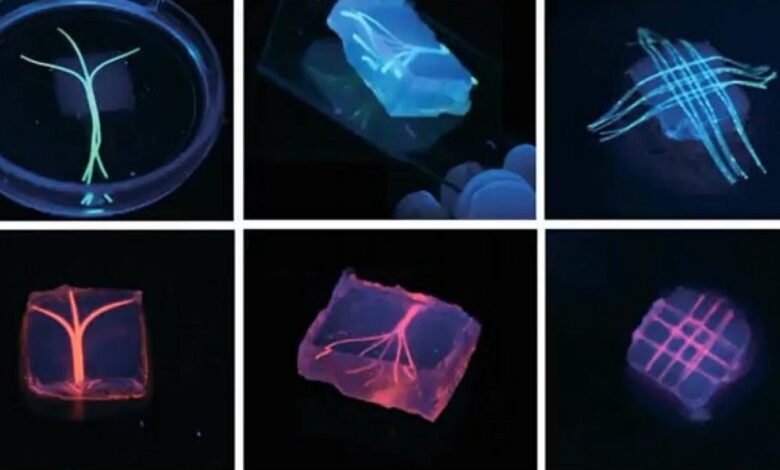
ما در تلاش بودهایم با چالشهای مختلفی در زمینه تولید مواد جدید با قابلیت تقلید ساختار و ویژگیهای نسوج بدن انسان دستوپنجه نرم کنیم و با کمک معماری بیومیمتیک (استفاده از مدلهای واقعی زیستی) سازههایی ایجاد کنیم و سلولهای مختلفی را که برای ایجاد نسوج مهندسیشده کاربردی موردنیاز هستند، کشت دهیم. بهویژه بهواسطه توسعه فناوریهای جدیدی که امکان ساخت نسوج پیشعروقی را فراهم میکنند، پیشرفت چشمگیری در زمینه چاپ سهبعدی نسوج داشتهایم، برای مثال شیوهای را برای کشت فداکارانه بافت پوششی درونی یا اپیتلیوم ابداع کردهایم و درعینحال شیوههایی برای ایجاد عروق خونی خودسرهمشونده با استفاده از جوهرهای زیستی خلق کردهایم.
منظورتان از کشت فداکارانه مجرای درونی رگ چیست؟
ایده اصلی کشت فداکارانه این است که میتوانیم ابتدا ساختارهایی شبیه مجرای درونی عروق خونی را چاپ کنیم و پسازآن میتوانیم سلولها را اطراف این سازه چاپشده قرار دهیم تا مدل سهبعدی آن شکل بگیرد. درنهایت نسوجی که در ابتدا چاپ شدهاند از کل سازه (که از قابلیت تخلخلی مشابه رگهای خونی برخوردار است) جدا میشوند و سلولها هویتی شبیه یک بافت طبیعی به دست میآورند، بههمیندلیل به این نسوج اولیه بافت فداکارانه میگوییم.
روند چاپ سهبعدی یک بافت چگونه است؟
معمولا برای ایجاد بافت از چاپ سلولها و مواد ژلاتینی استفاده میکنیم. میتوانیم از الگویی اولیه برای تعیین شکل بافت موردنظر استفاده کرده و سپس براساس این الگو بافت را چاپ کنیم. پسازآن بافت چاپشده بهصورت تدریجی در رآکتورهای زیستی تکامل پیدا میکند و امکان رشد سلولهای بیشتر در آن فراهم میشود تا درنهایت بافتی کاربردی حاصل شود.
در آزمایشگاهتان روی ساخت چه نوع ماده زیستی جدیدی متمرکز شدهاید؟
تولید مواد جدید همواره اصلیترین بخش از پژوهشهای ما بوده است و دائما بهدنبال موادی هستیم که بتوانند چالشهای مختلف زیستپزشکی را برطرف کنند. این مواد چسبهای زیستی، هیدروژلهای سلولپذیر (سلول در برابر این ماده واکنش دفاعی نشان نمیدهد) و الاستومرها (نوعی پلیمر با قابلیت ارتجاعی بالا) را شامل میشوند، برای مثال اکنون بر استفاده از پروتئینهایی طبیعی از قبیل الاستین، ژلاتین و کراتین برای ساخت زیستمواد نوآورانهای با ویژگیهای قابلتنظیم متمرکز شدهایم.
چرا کنترل رفتارهای سلولی یا محیط سلولی تا این اندازه در پروژههای شما اهمیت دارد؟
سلولها سیستمهایی زنده هستند. آنها با ریزمحیطی که احاطهشان کرده تعامل دارند و عملکردشان را متناسب با آن تغییر میدهند و فعالانه محیط خود را تعدیل میکنند. به بیانی دیگر اگر بهگونهای بتوانیم محیط سلول را تحتکنترل درآوریم، درواقع رفتارهای سلول را تحتکنترل درآوردهایم. بااینهمه این کار بهواسطه ابعاد کوچک سلولها بسیار دشوار است و کنترل رفتار آنها به ایجاد روشها، ابزارها و موادی نیازمند است که امکان دسترسی به ریزمحیط اطراف سلولها را برای ما فراهم آورد. این کار برای کنترل سرنوشت سلولها بسیار حیاتی است.
عملکرد چسبزخمهای هوشمند به چه صورت است؟
زخمهای مزمن محیطهایی پویا هستند که ویژگیهایشان بهسرعت تغییر میکند. ازاینرو درمان مناسب این زخمها به آگاهی دقیق از وضعیت زخم نیازمند است. ما نوعی پوشش را برای زخمها متصور شدیم که میتواند ویژگیهای مختلف بستر زخم را ارزیابی کرده و اطلاعات آن را بررسی کند. پسازاینکه چسبزخم هوشمند وضعیت زخم را درک کرد، میتواند داروهای موردنیاز و متناسب با این وضعیت را به زخم انتقال دهد. این پوشش همچنین میتواند با منبعی خارجی یا شبکهای بیسیم ارتباط برقرار کند و اطلاعات جمعآوریشده را به بیمارستانها و مراکز پزشکی انتقال دهد.
فکر میکنید ساخت اندامهایی پیچیده مانند قلب یا چشم در آینده نزدیک امکانپذیر است؟
شاید ساخت مدلهای سادهای از این اندامها در چندسال آینده امکانپذیر شود. بااینهمه ساخت اندامی با کیفیت اندام طبیعی و با عملکردی مشابه به زمان بیشتری نیاز دارد. پیشبینی اینکه ساخت اندامهای پیچیدهای مانند قلب چه زمانی امکانپذیر میشود، بسیار دشوار است، اما پیشرفتهای اخیر در زمینه زیستمواد، زیستچاپی، سلولهای بنیادین و زیستشناسی مولکولی قابلیتهای ما را تا حد چشمگیری افزایش داده است، ازاینرو میتوان گفت درنهایت ترکیب این پیشرفتها و پیشرفتهای بیشتر در این حوزهها، ساخت چنین اندامهای پیچیدهای را به واقعیت تبدیل خواهد کرد.
پیشرفت مهندسی نسوج و اندام از نظر شما از گذشته تابهحال چگونه بوده است؟
این حوزه علمی با حرکتی مثبت آغاز و در مدتی کوتاه به حوزه وسیع پژوهشی تبدیل شد. این حرکت روبهجلو، هرروز با مشاهده دستاوردهای هیجانانگیزی که به دست میآید و نتایجش در نشریات علمی معتبر منتشر میشود، ادامه دارد.
آیا تاکنون با گروهی از محققان ایرانی همکاری داشتهاید یا مقاله جالبی از ایران توجه شما را به خود جلب کرده است؟
ما در آزمایشگاهمان سابقه طولانیای در همکاری با دانشمندان ایرانی داریم و حتی میزبان چندین دانشمند ایرانی بودهایم که به همکاریهای متعدد و انتشار مقالههای مشترک و ادامه این همکاریها منجر شده است، علاوهبراین به نظر من چشمانداز دانش ایران درحالتوسعه است و مراکز علمی ایران مقالههای جالبتوجه فراوانی را منتشر میکنند.
با توجه به پروژههایی نظیر بافت روی تراشه، چسبزخم هوشمند و چاپ سهبعدی اندامها که در آزمایشگاهتان روی آنها متمرکز هستید، آینده طب شخصیسازیشده را چگونه میبینید؟
معتقدم هر بیمار چالشهای مختص به خود را دارد که این چالشها تحتفرمان ژنوم و شرایط محیطی هستند. ازاینرو معتقدم مفهوم طب عمومی که یک درمان را برای همه انسانها مناسب میپندارد، چندان مطلوب و تکاملیافته نیست. بههمیندلیل امیدواریم فناوریهایی خلق کنیم که زمینهساز تحقق طب شخصیسازیشده شوند، برای مثال سکوی اندام یا بافت روی تراشه بهتدریج به ما امکان خواهد داد که سلولهای خاص بیمار را کشت دهیم و واکنش این سلولها را نسبت به داروهای مختلف بررسی کنیم تا درنهایت بتوانیم بهترین وضعیت درمانی متناسب با هر بیمار را تعیین کنیم.
فکر میکنید فناوری اندام روی تراشه میتواند بهمرور به آزمایشهای حیوانی پایان ببخشد؟
ایده اصلی انجام پروژه اندام روی تراشه درواقع از همین مسئله نشات میگیرد؛ اینکه روزی آزمایشهای علمی روی حیوانات متوقف شود. بااینهمه دستیافتن به این هدف به مطالعات بیشتر و کسب مجوزهای معتبرتری نیاز دارد. در ابتدا از چنین سیستمهایی در کنار آزمایشهای حیوانی استفاده خواهد شد، اما در آینده ممکن است بهصورت کامل جایگزین آزمایشهای حیوانی شوند.
همانطورکه پیشتر هم به آن اشاره کردید، بیشتر مطالعاتتان بر شبیهسازی رفتار طبیعی سلولها یا محیط دربرگیرنده آنها متمرکز شده است تا بهواسطه این کار تاثیرگذاری درمانها یا داروها را افزایش دهید. در این مطالعات دقیقا چه بیماریهایی را هدف گرفتهاید؟
در تلاشایم تا بحرانیترین چالشهای پزشکی را هدف قرار دهیم، بهخصوص به ابداع شیوههایی برای درمان علائم مرتبط با بیماریهای سرطان و دیابت علاقهمندیم. علاوهبراین تلاشهای ما در زمینه مهندسی نسوج بهشدت بر بیماریهای قلبیعروقی و استخوانی متمرکز است.
آیا تاکنون حین مطالعاتتان بهواسطه تغییر کاربری یک فناوری، موفق شدهاید ابزار یا فناوری جدیدی ابداع کنید؟
تاکنون تعداد زیادی مواد جدید و فناوریهای نو را حین انجام مطالعاتمان ابداع کردهایم. همچنین در زمینه درک پیشرفتهای علمی و ترکیب فناوریهای مختلف با هدف رفع نیازهای موجود در حوزه عمومی مهندسی زیستپزشکی کاملا فعال هستیم. درحالحاضر روی تجهیزات پزشکیای مطالعه میکنیم که میتوان از آنها برای جراحی استفاده کرد؛ ازجمله چسبهایی که میتوان از آنها برای بستن زخمها استفاده کرد، یا موادی که مانع خونریزی میشوند.
No tags for this post.





