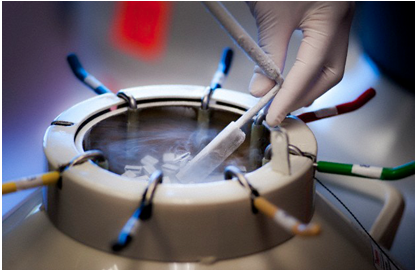
انجماد اسپرم گونههای دامی در محیط گیاهی
هفدهمین جشنواره بینالمللی تحقیقاتی رویان از روز چهارشنبه، 10 تا روز جمعه 12 شهریورماه در سالن رازی دانشگاه علوم پزشکی ایران برگزار میشود.در این جشنواره از 5 محقق خارجی از کشورهای چین، استرالیا و آمریکا و 3 محقق داخلی تقدیر به عمل میآید.
بر اساس رای داوران از بخش بینالملل، پروفسور ژیانگو ژائو از چین، پروفسور پیتر کوپمن از استرالیا، دکتر محمد شریف تابع بردبار از آمریکا، پروفسور میگوئل رامالهو سانتوس از آمریکا و پروفسور ژیائوهوآ شن از چین به عنوان محققان برتر این دوره از جشنواره بینالمللی تحقیقاتی رویان مورد تقدیر قرار خواهند گرفت.
در بخش داخلی نیز دکتر آناهیتا محسنی میبدی، دکتر کامران قائدی و دکتر محسن شرفی معرفی خواهند شد.
ارائه مدلهای حیوانی برای دو بیماری
به گزارش خبرنگار ایسنا، در تحقیقات زیست پزشکی، خوک به عنوان یک مدل حیوانی مناسب برای بیماریهای انسانی مورد استفاده قرار میگیرد. به این ترتیب ایجاد تغییرات ژنتیکی موثر و دقیق در این گونه، ساخت مدل برای بیماریهای مختلف را تسهیل میکند.
از سوی دیگر ظهور روشهای ویرایش ژنی همچون ZNFs ، TALENs و CRISPR/Cas9 فصل جدیدی در ایجاد حیوانات ژن مهندسی شده با هدف تولید مدل بیماریهای انسانی در حیوانات اهلی ایجاد شد. از این رو توسعه یک راهکار مهندسی ژنتیک با دقت و کارایی بالا که بتواند همزمان چند ژن را در ژنوم مدل حیوانی مورد نظر وارد و یا تخریب کند، میتواند ایجاد مدلهای حیوانی را تسریع بخشد.
در این راستا پروفسور ژیانگو ژائو از کشور چین و همکارانش با اجرای پروژهای با عنوان «ویرایش ژنتیکی با بازدهی بالا در خوک به منظور تولید مدل بیماریهای انسانی» نشان دادند که استفاده همزمان از تکنولوژی TALENs و شبیه سازی میتواند با کارایی بالا خوکهای ناکاوت دو آللی ایجاد کند.
علاوه بر آن، این گروه روشهایی برای انتخاب موثرترین sgRNA با استفاده از سیستم غربالگری در تکنیک CRISRR/Cas9 ایجاد کردند؛ به نحوی که میتوان ژن مورد نظر را به صورت دو آللی ناکاوت کرد. به این ترتیب این گروه موفق شدند با استفاده از تکنیک TALEN و CRISRR و با ویرایش ژنتیکی، مدلهای حیوانی برای بیماری پارکینسون و نقص شنوایی ارائه دهند.
این طرح دارای 3 مقاله منتشر شده در مجلات علمی با ضریب نفوذ بیش از 5.5 بوده است.
اثبات نقش رتینوئیک اسید در تقسیمات میوزی تخمدان
پروفسور پیتر کوپمن و همکارانش پیش از این نشان دادند که که رتینوئیک اسید در شروع میوز در سلولهای جنسی واقع در تخمدان جنین نقش کلیدی دارد، در حالی که سلولهای جنسی جای گرفته در بیضه در برابر مواجه شدن با رتینوئیک اسید حفاظت میشوند.
این یافته به معمای طولانی تفاوت در ورود میوز در جنسیتهای مختلف پایان بخشید.
ولی گروه دیگری از پژوهشگران ادعا کردند رتینوئیک اسید را در تخمدان جنینهای در حال تشکیلشدن، نیافتهاند و حتی تکامل طبیعی سلولهای جنسی در جنین موش مادهای که آنزیمهای سازنده رتینوئیک اسید در آن مهار شده باشند، امکان پذیر است.
به منظور پاسخ به این ادعا دکتر کوپمن و همکارانش در پژوهش تازهای با عنوان «تایید رتینوئیک اسید به عنوان القا کننده اصلی میوز در سلولهای جنسی جنینی» نشان دادند که حضور رتینوئیک اسید برای القای میوز در سلولهای جنسی جای گرفته در تخمدان ضروری است.
این یافته تاییدی بر نقش کلیدی رتینوئیک اسید در آغاز میوز در سلولهای جنسی بوده و به ابهامات ایجاد شده پاسخ داده است. این طرح دارای دو مقاله منتشر شده در مجلات علمی با ضریب نفوذ 11.5 بوده است.
ارائه راهکاری برای درمان بیماری دیستروفی
دیستروفی عضلانی نام گروهی از بیماریهای ژنتیکی است که بر اثر نقص در ژنهای کدکننده تعدادی از پروتئینهای مهم در ساختار فیبرهای ماهیچهای بروز میکند. این بیماری ارثی و پیشرونده است و در طول زمان ماهیچههای مختلف بیمار را درگیر کرده و توانایی ترمیم ماهیچه توسط سلولهای بنیادی نیز به تدریج کاهش پیدا میکند.
دیستروفی عضلانی دوشن (DMD) شدیدترین نوع دیستروفی عضلانی است که در اثر نقص در ژن تولیدکننده پروتئین «دیستروفین» به وجود میآید. علائم دوشن از جمله ضعف ماهیچهای و اختلال در راه رفتن در سنین کودکی بروز میکند و در نهایت از کارافتادگی ماهیچههای قلبی و تنفسی منجر به فوت بیمار خواهد شد.
این بیماری نسبتا شایع است و یک پسر در هر 3500 تولد به آن مبتلا است. دیستروفین بزرگترین ژن در ژنوم انسان است و همین اندازه بزرگ این ژن باعث دشواری و کندی روند پژوهش درخصوص نقایص آن بوده است.
به منظور حل این مشکل، دکتر شریف بردبار و همکارانش با اجرای طرح تحقیقاتی «ویرایش ژنتیکی دیستروفی عضلانی دوشن در عضلات و سلولهای عضلانی موش مبتلا در شرایط In Vine» از روش ویرایش ژنتیکی (gene edeiting) برای اصلاح ژن معیوب دیستروفین در سلولهای ماهیچه قلبی، ماهیچه اسکلتی و همچنین سلولهای بنیادی ماهیچهای موشهای مبتلا به دیستروفی عضلانی دوشن استفاده کردند.
برای ویرایش ژنتیکی، تکنولوژی CRISPR (کریسپر) مورد استفاده قرار گرفت و قسمت معیوب ژن دیستروفین از ژنوم سلولهای ماهیچهای موشهای مبتلا خارج شد. این تغییر ژنتیکی باعث احیای عملکرد ماهیچه در موشهای بیمار شد.
این روش امکان اصلاح دائمی نسخه داخلی ژن معیوب در بافتهای ماهیچهای را فراهم میکند و برخلاف روشهای مرسوم ژندرمانی، تولید پروتئین دیستروفین منوط به وجود همیشگی یک نسخه خارجی از ژن سالم در ماهیچه نخواهد بود. همچنین، این روش امکان اصلاح دائمی ژن معیوب در سلولهای بنیادی ماهیچهای موجود در عضلات اسکلتی را ایجاد میکند که باعث خودترمیمی به وسیله این سلولهای اصلاح شده در ماهیچه خواهد شد.
این طرح دارای یک مقاله منتشر شده در مجله علمی ساینس با ضریب نفوذ 33 بوده است.
بهبود تکنیکهای درمان ناباروری
یک لقاح موفق زمانی حاصل میشود که سلول اسپرم با سلول تخمک ادغام شود. در زمان لقاح، فقط DNAاسپرم که عاری از هیستون و پیچیده شده در پروتامینها است، وارد تخمک میشود؛ بنابراین لازم است تا مجدداً ساختار نوکلئوزومی را برای گذراندن دوره تکوین، به دست آورد. برنامهریزی مجدد کروماتینی ژنوم پس از لقاح اتفاق میافتد و به وسیله عوامل بیشمار و ناشناخته مادری کنترل میشود.
در پژوهشی که توسط دکتر میگوئل سانتوس و همکارانش با عنوان «نقش الحاق مولکول H3.3 با واسطه پروتئین Hira در همانندسازی DNA و رونویسی RNA ریبوزومی سلول زیگوت موش» انجام شد، با استفاده از ابزارهای ژنتیکی، مانند تکنیک ZP3-Cre و حذف مشروط الل Hira، ژن Hira به طور اختصاصی در حین تخمکزایی حذف شد.
برخلاف باور رایج میان دانشمندان که تصور میکردند رونویسی برای رشد و نمو تخم لازم نیست؛ نتایج این پژوهش نشان داد که رونویسی وابسته به Hira/H3.3 در RNA ریبوزومی برای تسهیم اول ضروری است. دکتر میگوئل سانتوس و همکارانش نشان دادند که الحاق H3.3 با واسطه پروتئین هیرا (Hira-mediated H3.3 incorporation) برای برنامهریزی مجدد ژنوم پدری در سلول تخم ضروری بوده و نقش غیرمنتظرهای در رونویسی RNA ریبوزومی در سلول تخم موش دارد.
این محققان به دفعات مشاهده کردند که جنینهای حاصل از ICSI (تزریق درون سیتوپلاسمی اسپرم) منتج از تخمک موشهای ماده فاقد پروتئین Hira، در مرحله پس از تشکیل تخم متوقف میشوند؛ در نتیجه یافتههای این مطالعه میتواند به بهبود تکنولوژیهای درمان ناباروری کمک کند.
این طرح دارای سه مقاله منتشر شده در مجلات علمی با ضریب نفوذ 6.5 تا 9.5 بوده است.
اثبات نقش ژنهای کدکننده بر تنظیم بیان ژنهای مجاور خود
در حالی که بیشتر ژنهای شناخته شده در پستانداران از جمله انسان، عامل تولید پروتئینها هستند، دستهای از ژنها که در سالهای اخیر مورد توجه قرار گرفتهاند، حاوی اطلاعاتی هستند که به شکل مولکولهای RNA رونویسی میشود؛ اما به تولید پروتئین ختم نمیشود. گروهی از این مولکولهای RNA که طول بلندتری دارند، RNAهای غیرکدکننده طویل یا IncRNA نامیده میشوند.
در ژنوم پستانداران هزاران ژن مولد RNAهای غیرکدکننده طویل یا IncRNA وجود دارند که حدوداً 20 درصد آنها در مجاورت ژنهای کدکننده پروتئین قرار گرفتهاند.
در پژوهشی که توسط دکتر ژیائوهوآ شن و همکارانش با عنوان «قوانین تنظیمی Cis برای RNAهای طویل غیرکدکننده در تنظیم نسخهبرداری از DNA و تمایز سلولهای بنیادی» انجام گرفت، نشان داده شد که این IncRNAها بر تنظیم بیان ژن مجاور خود تاثیر میگذارند، به طوری که مهار 75 درصد از این IncRNAها موجب کاهش فعالیت و بیان ژن مجاور میشود. تنظیم فعالیت ژن Evx1 به وسیله 1ncRNA مجاورش که Evx1 as نامیده میشود. مثالی از این فرایند است. این سازوکار تنظیم بیان ژنها میتواند نقش موثری در تمایز و حفظ بنیادینگی سلولهای بنیادی و نیز تکوین پستانداران بر عهده داشته باشد.
این طرح دارای دو مقاله منتشر شده در مجله Cell stem cell با ضریب نفوذ 22 بوده است.
برگزیدگان داخلی جشنواره
بهبود روشهای درمان ناباروری از سوی محققان کشور
به گزارش ایسنا ناهنجاریهای کروموزومی یکی از علل ناباروری محسوب میشوند. یکی از راههای تشخیص این ناهنجاریها، بررسی سیتوژنتیک سلولهای مرحله متافازی به وسیله رنگآمیزی گیمسا است. اما روشهای کاریوتایپینگ معمول برای تشخیص ناهنجاریهای کوچک کروموزمی مناسب نیستند.
دکتر آناهیتا محسنی میبدی و همکارانش در پروژه تحقیقاتی با عنوان «فواید استفاده از سیتوژنتیک مولکولی در تشریح ناهنجاریهای کروموزمی موثر در ناباروری مردان: از موارد نادر تا درمان» نشان دادند با بکارگیری روشهای سیتوژنتیک مولکولی همچون FISH و aCGH میتوان ناهنجاریهای کروموزمی پیچیده و کوچک را تشخیص داد.
به این ترتیب حتی امکان تشخیص موزائیسمهای کروموزمی با درصد کم فراهم خواهد شد. این یافته میتواند باعث بهبود روشهای PGDs و PNDs در مراکز درمان ناباروری شود.
این طرح دارای سه مقاله منتشر شده در مجلات علمی با ضریب نفوذ 4.59 بوده است.
موفقیت محققان در افزایش بازده کشت سلولهای پرتوان انسانی
یک مساله مهم در کشت و نگهداری سلولهای بنیادی پرتوان انسانی آسیبپذیری آنها در هنگام جدا شدن از کلونی است که منجر به آپاپتوز سلولها میشود. برای غلبه بر این مشکل، به طور معمول از مهارکننده ROCK استفاده میشود؛ اما باز هم زندهمانی و کلونیزایی سلولهای پرتوان به میزان مطلوب نیست.
دکتر کامران قائدی و همکارانش پیش از این در تحقیقات خود نشان داده بودند که استفاده از PPARgamma کلونیزایی و تکثیر را در سلولهای پرتوان موشی بهبود میبخشد.
برای تعمیم این یافته به سلولهای پرتوان انسانی، این گروه با اجرای پروژه «استفاده از پیوگلیتازون (Pioglitazone) به عنوان روشی جدید در افزایش کارایی کلونیزایی در کشت سلولهای پرتوان انسانی» از آگونیست PPARgamma به نام pioglitazone سود جستند. نتایج پژوهش دکتر قائدی و همکارانش نشان داد، استفاده از pioglitazone همراه با مهارکننده ROCK آپاپتوز سلولها را کاهش داده و کلونیزایی را نسبت به زمان استفاده تنها از مهارکننده ROCK دو تا سه برابر افزایش میدهد.
Pioglitazone باعث مهار فعالیت GSK3 شده و فعالیت بتا کاتنین و E-Cadherin در غشای سلول را القا میکند. از این یافته میتوان در راستای بهبود شرایط کشت سلولهای پرتوان انسانی و افزایش بازده کشت این سلولها استفاده کرد.
این طرح دارای یک مقاله منتشر شده در مجله علمی با ضریب نفوذ 5.57 بوده است.
انجماد اسپرم در محیطهای گیاهی
انجماد اسپرم، نگهداری و استفاده طولانیمدت از ذخایر ژنتیک در مراکز دامپروری را ممکن میکند. بهبود روشهای انجمادی امکان نگهداری طولانیتر و کارایی بهتر پس از ذوب را فراهم خواهد کرد. به همین علت روشهای انجمادی پیوسته در حال اصلاح و بهبود است.
به منظور ارتقای کیفیت انجماد اسپرم، دکتر محسن شرفی و همکارانش با اجرای طرح تحقیقاتی «بهینه کردن روش انجماد اسپرم حیوانات اهلی با استفاده از یک محیط انجمادی گیاهی جدید» یک نگهدارنده گیاهی را از «لیستین سویا» استخراج کرده و برای نخستین بار در جهان برای انجماد اسپرم در گونههای مختلف دامی مورد ارزیابی قرار دادند.
نخستین نتایج این پژوهش در سال 2010 توسط دکتر بردبار و همکارانش منتشر شد. پس از آن به سرعت پروژههایی از سوی همین گروه و سایر گروههای تحقیقاتی در دنیا در جهت افزایش کارایی آن اجرا شد که نتایج آنها نیز منتشر شد. هماکنون استفاده از این روش در انجماد اسپرم گاو، قوچ، بز و خروس به طور کامل اجرا و بهینه شده است و پژوهشگران به دنبال یافتن راهی برای تعمیم آن به انسان هستند. نتایج حاصل از این طرح در 15 مقاله بینالمللی از سال 2010 تاکنون به چاپ رسیده است و اکنون در مرحله تجاریسازی و ورود به بخش صنعت قرار دارد.به گزارش ایسنا، این طرح دارای 15 مقاله منتشر شده در مجلات علمی بوده است.
No tags for this post.





