به گزارش سیناپرس، محققان موسسه ملی بینایی آمریکا، با استفاده از ژن درمانی، توانسته اند، از نقص مژگان تحت تأثیر یک نوع بیماری چشمی نادر، در سلول های شبکیه جلوگیری کنند. آموروز مادرزادی لبر (LCA) یک بیماری چشمی نادر است که باعث نابینایی در اوایل کودکی می شود.
محققان با استفاده از ارگانوئیدهای شبکیه مشتق شده از بیمار، دریافتند که نوعی از LCA ناشی از جهش در ژن NPHP5 (که IQCB1 نیز نامیده می شود) نقایص شدیدی را در مژک اولیه، ایجاد می کند. این یافته ها نه تنها عملکرد پروتئین NPHP5 در مژک اولیه را روشن می کند، بلکه منجر به درمان بالقوه ای برای این وضعیت، می شود.
محققان گفته اند، کمبود NPHP5 باعث نابینایی زودرس می شود و در موارد شدیدتر، بسیاری از بیماران، علاوه بر تحلیل شبکیه، بیماری کلیوی را نیز تجربه می کنند. ما یک رویکرد ژن درمانی طراحی کرده ایم، که می تواند از نابینایی در کودکان مبتلا به این بیماری جلوگیری کرده و در صورت تحقیقات بیشتر، حتی به درمان سایر عوارض این بیماری نیز کمک کند.
LCA یک بیماری ژنتیکی نادر است که منجر به تخریب شبکیه حساس به نور در پشت چشم می شود. نوع LCA ناشی از جهش در NPHP5 نسبتا نادر است. به گزارش سیناپرس، این بیماری در تمام موارد منجر به نابینایی، و در بسیاری از موارد باعث نارسایی کلیه نیز می شود، وضعیتی که با عنوان سندرم Senior-Løken شناخته شده است.
تیم تحقیقاتی، نمونه سلول های بنیادی دو بیمار مبتلا به کمبود NPHP5 در مرکز بالینی NIH را مورد بررسی قرار دادند. این نمونه های سلول بنیادی برای تولید ارگانوئیدهای شبکیه، که دارای بسیاری از ویژگی های ساختاری و عملکردی شبکیه واقعی هستند، استفاده شدند.
ارگانوئیدهای شبکیه مشتق شده از بیمار، بسیار ارزشمند هستند، زیرا از ژنوتیپ و تظاهرات بیماری شبکیه در بیماران واقعی تقلید می کنند و محیط بافتی «شبه انسان» را برای آزمایش مداخلات درمانی، از جمله ژن درمانی، فراهم می کنند.
این ارگانوئیدهای شبکیه، نقایصی را در گیرنده های نوری، از جمله از دست دادن بخشی از گیرنده نوری به نام بخش های خارجی، نشان دادند. در یک شبکیه سالم، بخش های خارجی گیرنده نوری، حاوی مولکول های حساس به نور به نام اپسین هستند.
به گزارش سیناپرس، هنگامی که بخش خارجی، در معرض نور قرار می گیرد، گیرنده نوری سیگنال عصبی را آغاز می کند که به مغز می رود و بینایی را واسطه می کند. بخش خارجی گیرنده نور، نوع خاصی از مژک اولیه است، ساختاری قدیمی که تقریباً در تمام سلول های جانوری یافت می شود.
پروتئین NPHP5 در ساختار دروازه مانندی در پایه مژک اولیه قرار دارد که به فیلتر کردن پروتئین هایی که وارد مژک می شوند، کمک می کند. مطالعات قبلی روی موش ها، نشان داده است که NPHP5 در مژک دخیل است، اما محققان هنوز نقش دقیق NPHP5 در گیرنده نور مژک را نمی دانند و مشخص نیست که جهش ها چگونه بر عملکرد این پروتئین تأثیر می گذارند.
در مطالعه اخیر، محققان کاهش سطح پروتئین NPHP5 را در سلول های ارگانوئیدی شبکیه مشتق شده از بیمار و همچنین کاهش سطح پروتئین دیگری به نام CEP-290 را یافتند که با همکاری NPHP5، دروازه مژه اولیه را تشکیل می دهد.
علاوه بر این، بخش های خارجی گیرنده نوری در ارگانوئیدهای شبکیه، کاملاً از بین رفته بودند و پروتئین اپسین که باید در بخش های بیرونی جای می گرفت، درون بدنه سلول گیرنده نور یافت شد.
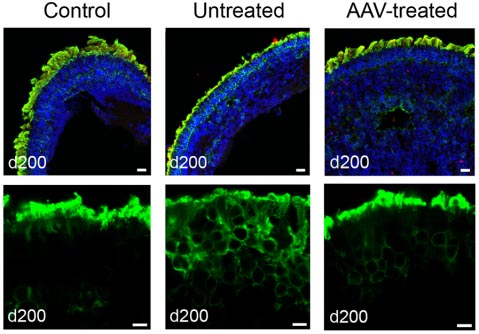
محققان با استفاده از یک ناقل ویروسی مرتبط با آدنو (AAV) حاوی نسخه عملکردی NPHP5، به عنوان یک وسیله ژن درمانی، بازسازی قابل توجهی از پروتئین اپسین متمرکز شده در محل مناسب خود، یعنی در بخش های خارجی ارگانوئیدهای شبکیه، را مشاهده کردند. یافته ها، همچنین نشان داده اند که NPHP5 عملکردی، ممکن است دروازه مژه اولیه را تثبیت کرده باشد.
به گزارش سیناپرس، نتایج تحقیقاتی در مجله Stem Cell Reports منتشر شده اند.
ترجمه: سنا دلفیه
No tags for this post.